

喜 报
2025年1月2日,腾业创投已投企业赛桥生物的重要合作伙伴——铂生卓越生物科技(北京)有限公司自主研发的“艾米迈托赛注射液”荣获国家药品监督管理局(NMPA)的上市批准,标志着我国首款获批上市的干细胞疗法的诞生,结束了我国间充质干细胞(MSC)药无上市产品的空白历史,并开启了干细胞商业化的新纪元。这一成就不仅成为我国干细胞疗法领域的重要里程碑,值得一提的是,“艾米迈托赛注射液”与2024年12月18日美国FDA首款获批的MSC药物几乎同时上市,预示着我国干细胞技术已走到全球前列,展现了我国在干细胞研究和临床应用方面的领先地位。

赛桥生物有幸为铂生卓越“艾米迈托赛注射液”提供了适应于商业化大规模生产的创新解决方案,为我国干细胞药物的快速工艺放大、无缝衔接、降本增效做出重要贡献。此外,赛桥生物目前还与多家头部企业携手推动商业化CAR-T的生产体系升级,加速推动免疫细胞药物的大规模商业化应用,让我国先进的细胞药物有机会服务更多患者。


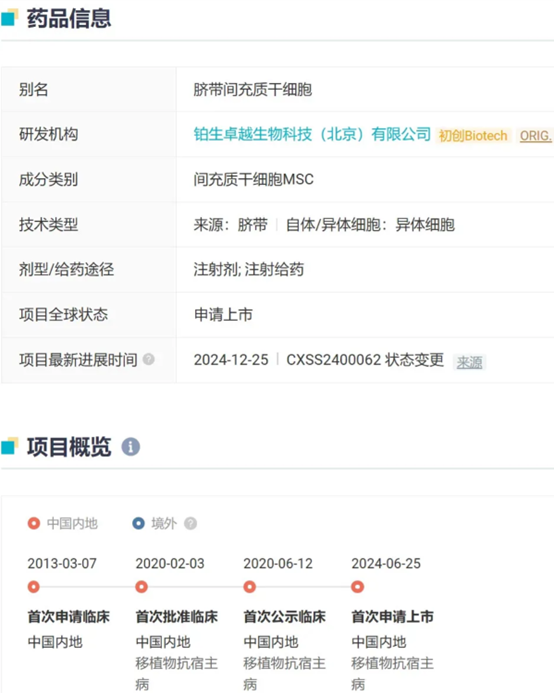
本品用于治疗 14 岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病。移植物抗宿主病是异基因造血干细胞移植后,来源于供者的淋巴细胞攻击受者组织发生的一类多器官综合征,表现为主要累及皮肤、胃肠道、肝、肺和黏膜表面的组织炎症、纤维化等。艾米迈托赛注射液系人脐带间充质干细胞注射剂。该品种的上市为相关患者提供了新的治疗选择。
赛桥生物作为全球极少数具备全自主知识产权和供应链的CGT新质生产力构建者,始终秉持着以客户为中心,以创新为本色的理念,积极探索和建立更加高效、简单、低成本的新质生产方式,为客户提供更多的工艺突破、降本增效和产业化解决方案。未来,赛桥生物将继续通过生产工艺与生产设备的一体化创新,解决细胞基因药物在生产制造工艺开发、大规模生产、质量控制和稳定性等方面的技术难题。推动癌症和退行性疾病的细胞基因治疗从百万元进入万元时代,惠及更广大的患者。